聚合硫酸鐵的合成方法(七)氧氣一催化氧化法
發(fā)布時(shí)間:2013/1/9 9:44:35 瀏覽次數(shù): 來源:m.yuhaotech.cn
聚合硫酸鐵的合成方法,氧氣一催化氧化法
氧氣是一種較強(qiáng)的氧化劑[V(O
2/H
2 O)+O
2 =1. 23],它可以將硫酸亞鐵直接氧化成堿式硫酸鐵,反應(yīng)方程如下:
4FeSO4 +2H2 O+O2 =4Fe(OH)SO4
此反應(yīng)在空氣中就能緩慢地進(jìn)行,但在酸性液中氧氣氧化硫酸亞鐵的速度非常慢,例如向含硫酸亞鐵50%、硫酸IO%的水溶液中鼓入氧氣,經(jīng)7h反應(yīng)后,亞鐵離子仍沒有氧化成三價(jià)鐵離子。據(jù)文獻(xiàn)報(bào)道,氧氣氧化硫酸亞鐵的反應(yīng)速度方程為:
[Fe2+]dt=k[Fe2+][O2] pH<1
即亞鐵的氧化速度與亞鐵濃度和氧氣濃度成正比,如果液體中氧氣的濃度為定值,則上述方程可簡化為:
[Fe2+]/dt=k′[Fe2+] pH<1 (1-1)
根據(jù)氧化實(shí)驗(yàn)
[Fe2+]/dt=0 pH<1 (1-2)
對比式(1-1)和式(1-2)可知k’是一個(gè)趨向于零的常數(shù),也就是說以純氧直接氧化硫酸亞鐵的溶液,反應(yīng)速度很慢,以至于趨向于零。為加快氧氣氧化硫酸亞鐵的速度,經(jīng)過多次實(shí)驗(yàn)篩選,選擇合理的催化劑,進(jìn)行催化氧化實(shí)驗(yàn),反應(yīng)方程式為:
H2 SO4 +2NaNO2 =2HNO2 +Na2 SO4
H2 SO4 +2HNO2 +2FeSO4 =Fe2 (SO4)3+2NO+2H2O
2NO+O2 =2NO2
H2 SO4 +NO2 +2FeSO4 =Fe2 (SO4 )3+NO↑+H2O
總反應(yīng)總式為
4FeSO4·7H2 O+(2 -72)H2 SO4 +O2 =2Fe2 (OH)n(SO4)3-n / 2 +(3O-2n) H2O
(注:所有反應(yīng)式中n<2)
對上述反應(yīng)的影響因素較多,我們著重研究了反應(yīng)溫度、反應(yīng)壓力、攪拌速度對反應(yīng)速度的影響,從而確定影響反應(yīng)速度的主要因素或者說決定反應(yīng)速度的控制步驟。
(1)溫度的影響硫酸亞鐵的溶解度隨溫度變化很大,在63℃時(shí),硫酸亞鐵的濃度可以達(dá)到10%,加入過量的硫酸亞鐵就能形成飽和溶液,使溶液中亞鐵離子濃度高于11%,因此反應(yīng)溫度應(yīng)控制在63℃以上。根據(jù)反應(yīng)速度公式,反應(yīng)物濃度越高反應(yīng)速度越快,因此可以盡可能地提高亞鐵離子的濃度。由于產(chǎn)品標(biāo)準(zhǔn)規(guī)定聚合硫酸鐵中三價(jià)鐵離子含量為11%,在高于63℃時(shí),就能將溶液中三價(jià)鐵離子的濃度控制在這一范圍內(nèi),因此反應(yīng)溫度過高對于反應(yīng)并無好處,考慮到反應(yīng)過程中由于熱量損失引起溶液結(jié)晶,溫度應(yīng)稍高于63℃,一般將溫度控制在80℃以下就能保證反應(yīng)的順利進(jìn)行。
(2)攪拌速度的影響氧化聚合反應(yīng)在不同的攪拌速度下,于5孔圓底燒瓶中進(jìn)行。5個(gè)孔分別為攪拌孔、測溫孔、加氧孔、加催化劑孔、排氣孔。通過水浴加熱,將溫度控制在65℃。按照亞鐵離子為11%,鹽基度為10%投加適量的硫酸亞鐵、硫酸和水,每次反應(yīng)投加的硫酸亞鐵總量為定值。圖3—25為攪拌速度不同時(shí)硫酸亞鐵氧化成三價(jià)鐵的百分含量與時(shí)間的關(guān)系圖。
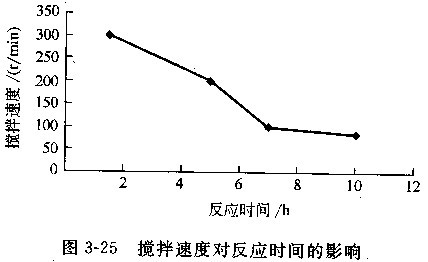
從圖中可以看出反應(yīng)過程中,隨攪拌速度提高,亞鐵完全氧化所需的時(shí)間縮短,這說明對于上述氣液反應(yīng),攪拌速度提高。產(chǎn)生較大的比表面積,氣液接觸充分,使氣相中的催化劑和氧氣擴(kuò)散到液體表面的速度加快,從而使氧化速度升高。
(3)反應(yīng)壓力的影響化學(xué)反應(yīng)中提高反應(yīng)物的濃度可以加快反應(yīng)的進(jìn)行。對于有氣體參加的化學(xué)反應(yīng),例如氧氣氧化硫酸亞鐵的過程,可以提高氣液相壓力,以達(dá)到升高氣相濃度以及在液相中的溶解度,加快反應(yīng)的目的。為此我們在攪拌速度相同而壓力不同的條件下,在反應(yīng)釜中進(jìn)行硫酸亞鐵的氧化實(shí)驗(yàn)。結(jié)果見圖3-26。
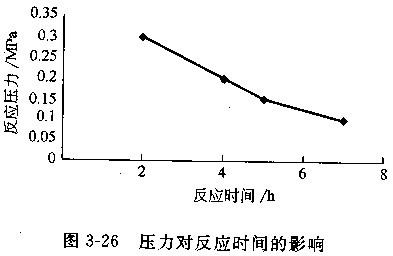
每個(gè)實(shí)驗(yàn)攪拌速度為l00r/min。通過圖3-26可以看出,在硫酸亞鐵濃度、攪拌速度等條件相同時(shí),隨著壓力的增大,反應(yīng)速度加快。由于液相體積難于壓縮,加大壓力只是增大了氣相的濃度和氣相在液相中的溶解度,從而加快了反應(yīng)的進(jìn)行。
對比圖3-25和圖3-26發(fā)現(xiàn),在常壓條件下攪拌速度為l00r/min,反應(yīng)時(shí)間為7h,攪拌速度為400r/min,反應(yīng)時(shí)間為4h。如果同在l00r/min攪拌速度進(jìn)行反應(yīng),提高壓力至o.2MPa,反應(yīng)時(shí)間為6h,遠(yuǎn)不如增大攪拌速度對反應(yīng)時(shí)間的影響明顯。另外從上述分析可知硫酸亞鐵的催化氧化過程是一個(gè)氣相傳質(zhì)控制的過程,即反應(yīng)過程中氣體的溶解過程控制了氧化聚合反應(yīng)速度,因此加快氣體的溶解就能提高反應(yīng)速度,縮短生產(chǎn)周期。為此有兩種 方法可供選擇,一是提高反應(yīng)壓力,二是采取 措施增大氣液反應(yīng)比表面積。硫酸亞鐵和硫酸的混合液是一種強(qiáng)腐蝕性液體,采用提高壓力方法的缺點(diǎn)一是對設(shè)備耐腐蝕性要求很高;二是操作不方便。另外,從前面分析可以知道提到壓力的效果不如增大氣液接觸比表面積的效果明顯。為了增大氣液接觸比表面積、加快反應(yīng)速度,用反應(yīng)釜生產(chǎn)時(shí),可以加快攪拌速度,增大氣液接觸比表面積。但此方法有一缺陷,一即反應(yīng)結(jié)束后剩余氣體必須排放,造成污染,因此必須增加氣體處理設(shè)備。另外采用反應(yīng)釜生產(chǎn)時(shí),由于硫酸亞鐵中常混有砂石等雜質(zhì),在生產(chǎn)過程中設(shè)備磨損很嚴(yán)重。
(4)生產(chǎn)工藝
聚合硫酸鐵根據(jù)用氧氣氧化硫酸亞鐵反應(yīng)的特點(diǎn),我們采用了耐腐蝕材料制成反應(yīng)塔,利用混合液體在塔內(nèi)流動時(shí)形成的巨大比表面積,加強(qiáng)氣體的吸收,從而加快反應(yīng)速度。利用反應(yīng)塔進(jìn)行生產(chǎn)既可以在常壓,也可以在低壓條件下進(jìn)行,生產(chǎn)操作既安全又方便。
聚合硫酸鐵 的生產(chǎn)過程如下:按比例將硫酸亞鐵、硫酸和水加入溶解槽中,升溫至65~80℃,一用耐腐蝕泵將溶液打人反應(yīng)塔內(nèi),調(diào)節(jié)液體流量,使液體處于循環(huán)狀態(tài),同時(shí)向塔內(nèi)加入氧氣和催化劑,混合液即發(fā)生催化氧化聚合反應(yīng)。
聚合硫酸鐵 反應(yīng)過程中可以通過溶解槽夾套用蒸汽加熱,并不斷對反應(yīng)液中的亞鐵離子進(jìn)行監(jiān)測,待亞鐵離子完全氧化后,反應(yīng)結(jié)束,將液體
聚合硫酸鐵成品輸送到成品池。在反應(yīng)過程中雜質(zhì)被過濾器濾掉,不會對設(shè)備帶來磨損腐蝕問題。另外反應(yīng)結(jié)束后,未反應(yīng)的酸性氣體進(jìn)入反應(yīng)塔,用于下批物料的生產(chǎn),從而提高了
聚合硫酸鐵 原料的利用率,解決了污染問題。
實(shí)踐證明此
聚合硫酸鐵 新技術(shù)具有下列特點(diǎn):①反應(yīng)速度快,生產(chǎn)周期短,效率高,適于大規(guī)模生產(chǎn);②產(chǎn)品質(zhì)量優(yōu)良,達(dá)到并超過國家標(biāo)準(zhǔn)及化工部標(biāo)準(zhǔn);③生產(chǎn)可以在常壓或低壓下進(jìn)行,操作方便,安全;④生產(chǎn)原材料價(jià)格低,利用率高,降低了生產(chǎn)成本;⑤生產(chǎn)過程無三廢問題。
長期運(yùn)行證明,以反應(yīng)塔為反應(yīng)器生產(chǎn)
聚合硫酸鐵的新技術(shù)是一種非常理想的生產(chǎn)工藝,國內(nèi)尚無此類技術(shù)。它的應(yīng)用為我國
聚合硫酸鐵的生產(chǎn)開辟了新的途徑。同時(shí)
聚合硫酸鐵用于凈水處理的結(jié)果證明,
聚合硫酸鐵完全可以取代目前的無機(jī)低分子水處理劑,有著良好的經(jīng)濟(jì)效益和社會效益。
了解更多關(guān)于聚合硫酸鐵 的相關(guān)信息,請關(guān)注官網(wǎng):m.yuhaotech.cn



